
科目: 来源: 题型:选择题
| A. | 某烷烃的结构为: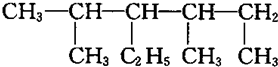 ,正确的命名是3,5-二甲基-4-乙基己烷 ,正确的命名是3,5-二甲基-4-乙基己烷 | |
| B. | 涤纶是由对苯二甲酸(PTA)和乙二醇(EG)通过加聚反应得到的 | |
| C. | 有机物CH3CH2CH(CH3)2的一氯代物有4种 | |
| D. | 有机同系物具有相同的通式,且组成相差若干个“CH2”,因此等质量的同系物燃烧耗氧相差物质的量为1.5nmol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X、Z两种元素可形成X2Z和X2Z2两种常见共价化合物 | |
| B. | M与Z形成的化合物的分子式为M2Z3 | |
| C. | 工业上可用电解熔融的W的氯化物的方法制取W的单质 | |
| D. | Z元素对应的单质与W元素对应的单质在不同条件下反应产物可能不同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 实验室中可用燃烧法处理CO、H2、H2S等可燃性尾气 | |
| B. | 检验硫酸亚铁铵晶体中是否含有结晶水:取一试管,用药匙加入2克硫酸亚铁铵晶体,并在试管口塞上一团蘸有少量无水硫酸铜粉末的棉花,同时塞紧塞子,点燃酒精灯加热试管,观察现象 | |
| C. | 取一药匙铁粉、半药匙食盐置于一片塑料薄膜上,混合均匀,滴一滴管水,包起塑料薄膜(不包紧,有空气),用手摸立刻有发烫感 | |
| D. | 在中和滴定实验中,既可用标准溶液滴定待测液,也可用待测液滴定标准溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 光导纤维、防弹玻璃、氧化铝陶瓷、硅藻土都是无机非金属材料,PLA、PE、橡胶、酚醛树脂都是人工合成高分子材料 | |
| B. | 贮氢金属并不是简单地吸附氢气,而是通过化学反应贮存氢气 | |
| C. | 科学家发现一种新的CO2晶体,该CO2晶体具有极强的硬度,是由CO2分子构成的空间立体网状结构 | |
| D. | 最新的氯碱工业是用离子交换膜电解槽电解饱和食盐水来生产氢气、氯气和烧碱的,电解槽中的离子交换膜既可以用阳离子交换膜也可以用阴离子交换膜 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 放电时负极反应为:3Zn-6e-═3Zn2+ | |
| B. | 放电时正极反应为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- | |
| C. | 放电时每转移3mol电子,正极有1mol K2FeO4被氧化 | |
| D. | 放电时负极附近溶液的碱性减弱 |
查看答案和解析>>
科目: 来源: 题型:解答题
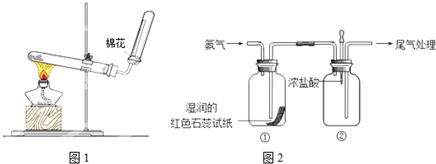
查看答案和解析>>
科目: 来源: 题型:解答题
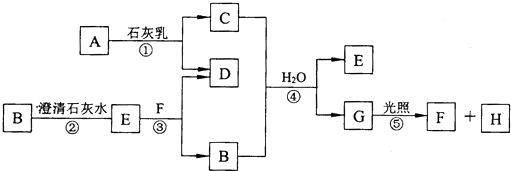
查看答案和解析>>
科目: 来源: 题型:解答题
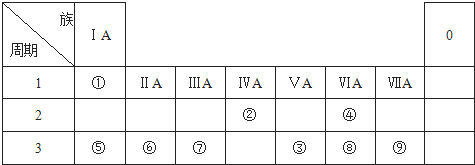
 ;元素⑦的原子结构示意图
;元素⑦的原子结构示意图 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ | |
| B. | 用大理石与稀盐酸制备二氧化碳:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| C. | 用氢氧化钠溶液吸收氯气:Cl2+2OH-=ClO-+Cl-+H2O | |
| D. | 铜片放入稀硝酸中产生气体:Cu+4H++2NO${\;}_{3}^{-}$=Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cu2+、H+、SO42-、Cl- | B. | Na+、Ba2+、NO3-、CO32- | ||
| C. | Al3+、H+、CO32-、Cl- | D. | Ba2+、OH-、Fe2+、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com