
科目: 来源: 题型:填空题
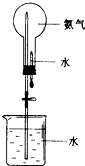 哈伯因为氨气的合成曾获1918年诺贝尔奖.
哈伯因为氨气的合成曾获1918年诺贝尔奖.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 ,过氧化氢
,过氧化氢
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al | B. | Al(OH)3 | C. | AlCl3 | D. | Al2O3 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 滴加试剂 | 所根据的现象 | 结论 |
| 不是盐酸 |
查看答案和解析>>
科目: 来源: 题型:解答题
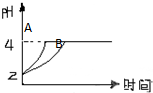 平衡原理探究题
平衡原理探究题| 滴加试剂及量 | 所根据的现象 | 结论 |
| 是盐水解之故 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com