
科目: 来源: 题型:多选题
| A. | 向硝酸钙溶液里滴加稀盐酸得到pH=4的溶液中:2c(Ca2+)=c(NO3-) | |
| B. | 将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸等体积混合所得的碱性溶液中(A-为酸根离子): c(Na+)>c(A-)>c(C1-)>c(OH-) | |
| C. | 0.1 mol/LNaAlO2溶液中:c(Na+)>c(AlO2-)>c(OH-)>c(H+) | |
| D. | 浓度均为0.1 mol•L-1的CH3COOH、CH3COONa的混合溶液中:2c(OH-)=2c(H+)+c(CH3COOH) |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 标准状况下,16g O2和O3混合物中所含原子数为NA | |
| B. | 标准状况下,等体积 Cl2和CCl4中所含氯原子数为1﹕2 | |
| C. | 常温常压下,14g N2含有电子数为7NA | |
| D. | 28g CO与22.4L CO2所含的碳原子数均为NA |
查看答案和解析>>
科目: 来源: 题型:解答题
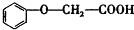 发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题:
发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题: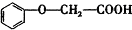 的分子式为C8H8O3.
的分子式为C8H8O3.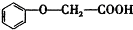 有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为
有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为 、
、 、
、 (其中一种)(任写一种).
(其中一种)(任写一种).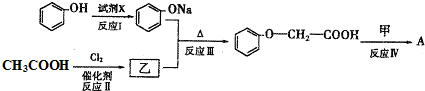
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H+、Fe2+、NO3-、SO42- | B. | Na+、H+、AlO2-、HCO3- | ||
| C. | Ca2+、Fe3+、CO32-、CH3COO- | D. | Ca2+、Na+、HCO3-、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,5.6L CCl4含有的分子数为0.25 NA | |
| C. | 在标准状况下,2.8g N2和2.24LCO所含质子数均为1.4NA | |
| D. | 常温下,1 L pH=1的硫酸溶液中含有的H+数为0.05NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl2和H2O2都能使品红溶液褪色 | |
| B. | 漂白粉和亚硫酸钠固体长期暴露在空气中变质 | |
| C. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| D. | SO2和Na2SO3溶液都能使溴水褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com