
科目: 来源: 题型:选择题
| A. | ①②③⑤⑧ | B. | ②④⑥⑦⑧ | C. | ①③⑤⑥⑦ | D. | ①②④⑧ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A.Cl2与CH4取代反应后的产物: | 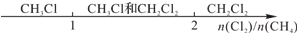 |
| B.向烧碱液中通入SO2后的产物: |  |
| C.铁与稀硝酸反应: | 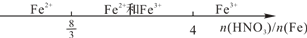 |
| D.向AlCl3溶液中滴加NaOH溶液,铝元素的存在形式: |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.008889 | B. | 0.08000 | C. | 0.1200 | D. | 0.2400 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH>7时,c(C6H5O-)>c(K+)>c(H+)>c(OH-) | |
| B. | pH<7时,c(K+)>c(C6H5O-)>c(H+)>c(OH-) | |
| C. | V[C6H5OH(aq)]=20ml时,c(C6H5O-)+c(C6H5OH)=2c(K+) | |
| D. | V[C6H5OH(aq)]=10ml时,c(K+)=c(C6H5O-)>c(OH-)=c(H+) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径:A>B>D>C | B. | 原子的最外层电子数目:A>B>D>C | ||
| C. | 原子序数:d>c>b>a | D. | 离子半径:C2->D->B+>A2+ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10℃时的HCl和H2O | B. | 400K时的水和CO2 | ||
| C. | 20℃时的氧气和空气 | D. | 常温下的H2和N2 |
查看答案和解析>>
科目: 来源: 题型:解答题
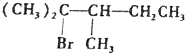 ,试推导A的构造式,用“*”标出手性碳原子,并用系统命名法命名.
,试推导A的构造式,用“*”标出手性碳原子,并用系统命名法命名.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 还原性 F->Cl->Br- | B. | 碱性:Na(OH)2>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性 HClO4>HBrO4>HIO4 | D. | 稳定性 HCl>H2S>PH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com