
科目: 来源: 题型:选择题
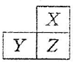 X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X,Y,Z是三种短周期的主族元素,在周期表的位置如图,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )| A. | 原子半径:X>Y>Z | |
| B. | 气态氢化物的热稳定性:X<Z | |
| C. | Y和Z的最高价氧化物对应水化物均为强酸 | |
| D. | X和Z形成的化合物只有共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
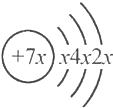 ,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )
,b与c形成的化合物的化学式为b3c,且b、c离子有相同的电子层结构,下列比较中,正确的是( )| A. | 原子序数:a>b>c | B. | 氢化物的稳定性:a>c>d | ||
| C. | 原子半径:d>a>c | D. | 最高价含氧酸的酸性:d>c>a |
查看答案和解析>>
科目: 来源: 题型:解答题
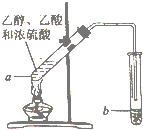 用如图所示的实驗装置制备少置乙酸乙酯.请回答有关问题:
用如图所示的实驗装置制备少置乙酸乙酯.请回答有关问题: CH3COOC2H5+H2O,反应类型是酯化反应(或取代反应).
CH3COOC2H5+H2O,反应类型是酯化反应(或取代反应).查看答案和解析>>
科目: 来源: 题型:填空题
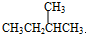 与
与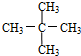 G.
G.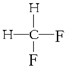 与
与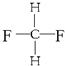
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | B. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | ||
| C. | Fe3O4+3CO$\frac{\underline{\;高温\;}}{\;}$3Fe+3CO2 | D. | MgO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
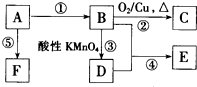 已知A、B、C、D、E、F是中学化学中常见的六中有机物,它们的转化关系如图所示(部分物质已省略).其中A是一种生物生长调节剂,E具有水果香味,F是一种可制成多种包装材料的高分子化合物.
已知A、B、C、D、E、F是中学化学中常见的六中有机物,它们的转化关系如图所示(部分物质已省略).其中A是一种生物生长调节剂,E具有水果香味,F是一种可制成多种包装材料的高分子化合物.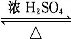 CH3COOC2H5+H2O;⑤nCH2=CH2$\stackrel{催化剂}{→}$
CH3COOC2H5+H2O;⑤nCH2=CH2$\stackrel{催化剂}{→}$ .
.查看答案和解析>>
科目: 来源: 题型:填空题
| 元素编号 | 元素性质或原子结构 |
| T | 最高正价与最低负价的代数和为4 |
| X | 最外层电子数是次电子数次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| Z | 最高正价是+7价 |
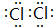 ;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).
;Y的氢化物的水溶液显碱性的原因为NH3+H2O?NH3•H2O?NH4++OH-(用离子方程式表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com