
科目: 来源: 题型:选择题
| A. | 用H2O2分解制O2,加入1~2滴FeCl3溶液,反应速率加快 | |
| B. | 在金属钠与足量水反应中,增加水的量能加快反应速率 | |
| C. | 一定条件下的反应:2SO2+O2?2SO3中,SO2的转化率能达到100% | |
| D. | 用铁和稀硫酸制取氢气,将稀硫酸换成浓硫酸可以加快反应速率 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 绿色化学的核心就是如何对被污染的环境进行无毒、无害化的治理 | |
| B. | 海水化学资源丰富,利用蒸馏的方法可以获得NaCl、Br2和Mg等物质 | |
| C. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| D. | 动物体内葡萄糖被氧化成H2O、CO2的同时,伴随着热能转变成化学能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 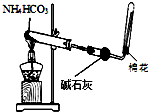 图装置用于制取少量的氨气 | |
| B. | 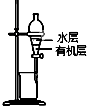 图装置用于提取I2的CCl4溶液中的I2 | |
| C. | 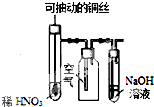 图装置微热稀HNO3,在广口瓶中可收集NO气体 | |
| D. | 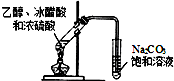 图装置可制取少量的乙酸乙酯 (夹持物略) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 因为盐酸的酸性强于氢硫酸,所以氯元素的非金属性强于硫 | |
| B. | 因为醋酸电离吸热,所以用NaOH溶液恰好中和等体积等浓度的醋酸和盐酸,前者放出热量少 | |
| C. | 钠的金属性比钾强,工业上用钠制取钾(Na+KCl?K↑+NaCl) | |
| D. | 因为某吸热反应能自发进行,所以该反应是熵减反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2、Br2、Cl2、酸雨 | B. | NH3、CO2、NO2、雾 | ||
| C. | HCl、SO2、N2、粉尘 | D. | SO2、NO2、CO、烟尘 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可加快产生氢气的速率 | |
| B. | 对于反应2H2O2═2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率 | |
| C. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气产生 | |
| D. | 100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单位时间内生成nmolO2的同时,生成2nmolNO2 | |
| B. | NO2?NO?O2反应速率的比为2:2:1 | |
| C. | 混合气体的颜色不再改变的状态 | |
| D. | 混合气体的压强不再改变的状态 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ag2O为电池的正极 | B. | Al在电池反应中被氧化 | ||
| C. | 电子由Ag2O极经外电路流向Al极 | D. | 溶液中的OH-向Al极迁移 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 非金属性:F>O>S | B. | 金属性:Rb>K>Li | ||
| C. | 稳定性:PH3>H2S>HCl | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com