
科目: 来源: 题型:选择题
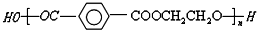 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 羊毛与该聚酯纤维的化学成分相同 | |
| B. | 该聚酯纤维和羊毛在一定条件下均不能水解 | |
| C. | 合成该聚酯纤维的单体为对苯二甲酸和乙二醇 | |
| D. | 由单体合成该聚酯纤维的反应属加聚反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2=CH-CH2-CH3和 | B. |  与 与 | ||
| C. | 分子组成都为 CnH2nO2 的物质 | D. | CH3CH2Cl与CH3CH2CH2Cl |
查看答案和解析>>
科目: 来源: 题型:解答题

 ,F
,F .
. .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 两溶液中n (H+)相等 | B. | 两溶液中c(Cl-)相等 | ||
| C. | 两溶液中c(OH-)相等 | D. | 两溶液中水的电离程度相等 |
查看答案和解析>>
科目: 来源: 题型:解答题
 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物其晶胞结构如右图所示,B离子均在晶胞体内,D的离子分占在晶胞顶点和面心.请回答下列问题.
有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物,D与B可形成离子化合物其晶胞结构如右图所示,B离子均在晶胞体内,D的离子分占在晶胞顶点和面心.请回答下列问题.查看答案和解析>>
科目: 来源: 题型:解答题
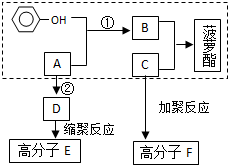 已知方框内是食品香精菠萝酯的生产路线,A、B又能发生方框外所示的转化关系.A、B、C的分子式分别C2H3ClO2、C8H8O3、C3H6O.信息:-OH和碳碳双键不能连在同一个碳原子上.
已知方框内是食品香精菠萝酯的生产路线,A、B又能发生方框外所示的转化关系.A、B、C的分子式分别C2H3ClO2、C8H8O3、C3H6O.信息:-OH和碳碳双键不能连在同一个碳原子上.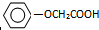 ;E
;E .
. .
.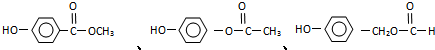 (有几种填写几种).
(有几种填写几种).查看答案和解析>>
科目: 来源: 题型:解答题
 夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.如图1是北京鸟巢试放烟火奥运五环图,并回答下列问题:
夜幕降临,北京奥运会主会场“鸟巢”内灯火辉煌,鼓瑟齐鸣.璀璨的烟花在空中组成奥运五环等图案,与场内表演相呼应.鸟巢夜景照明由五个部分组成,其中主体照明以传统文化元素“中国红”为主色.如图1是北京鸟巢试放烟火奥运五环图,并回答下列问题: ,C、D均为原子晶体,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C、D均为原子晶体,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:查看答案和解析>>
科目: 来源: 题型:填空题
 现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.
现有A、B、C、D、E、F六种物质或粒子,其中A、B、C、D都具有如图所示的结构或结构单元,(图中正四面体以外可能有的部分未画出,虚线不表示化学键或分子间作用力,X、Y可以相同也可以不同).A、B的晶体类型相同.单质A的同素异形体能与B物质发生置换反应.C、D、E、F含有相等的电子数,且D是阳离子,D与F的组成元素相同.C、E、F的晶体类型相同,由E构成的物质常温下呈液态.查看答案和解析>>
科目: 来源: 题型:解答题
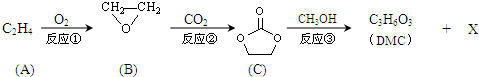
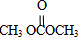 ;XOHCH2CH2OH;
;XOHCH2CH2OH;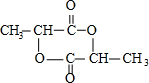 ;
;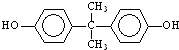 )在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n
)在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n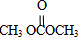 +n
+n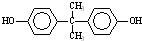 →
→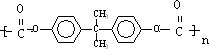 +4nCH3OH.
+4nCH3OH.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com