
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 | |
| B. | D元素处于元素周期表中第3周期第IV族 | |
| C. | C的最高价氧化物中含有共价键 | |
| D. | 四种元素的原子半径:A>B>D>C |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 催化剂V2O5,不改变该反应的逆反应速率 | |
| B. | 将2 mol SO2与2 mol O2放人密闭容器中,最终生成2mol SO3 | |
| C. | 在t1、t2时刻,SO2(g)的浓度分别是C1、C2,则时间间隔t1-t2内,SO2(g)消耗的平均速率为v=$\frac{{C}_{1}-{C}_{2}}{{t}_{2}-{t}_{1}}$ | |
| D. | 该反应是放热反应,则SO2的能量一定大于SO3的能量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑥ | C. | ①⑤⑥ | D. | ①②⑥ |
查看答案和解析>>
科目: 来源: 题型:填空题

 .
. .
. +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O.
+NaCl+H2O. +(2n-1)H2O.
+(2n-1)H2O. (写出其中一种结构简式).
(写出其中一种结构简式). )的合成路线示意图.
)的合成路线示意图.
查看答案和解析>>
科目: 来源: 题型:填空题
 △H=-116kJ•mol-1
△H=-116kJ•mol-1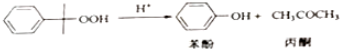 △H=-253k•mol-1
△H=-253k•mol-1
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 异丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
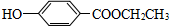 与足量NaOH溶液反应:
与足量NaOH溶液反应:
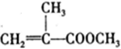 $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$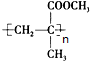
 )的反应:nCH2=CH-CN+nCH3COOCH=CH2$\stackrel{一定条件下}{→}$
)的反应:nCH2=CH-CN+nCH3COOCH=CH2$\stackrel{一定条件下}{→}$ .
.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH4O、C3H4O | B. | C2H4、C2H4O2 | C. | C3H6O3、CH2O2 | D. | C2H2、C2H6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com