
科目: 来源: 题型:选择题
| A. | CuSO4溶液能使蛋白质变性 | |
| B. | 糖类、油脂和蛋白质都属于高分子化合物 | |
| C. | 油脂有油和脂肪之分,但都属于酯 | |
| D. | 淀粉、油脂和蛋白质都能发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
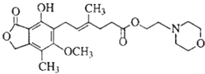
| A. | MMF能与碳酸钠溶液反应放出气体 | |
| B. | 1molMMF能与6mol氢气发生完全加成 | |
| C. | MMF遇三氯化铁溶液显紫色 | |
| D. | 1molMMF能与2molNaOH溶液完全反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  | |
| B. | 2CH3CH2+O2$→_{△}^{Cu}$2ch3CHO+2H20 | |
| C. | ClCH2=CH2+NaOH$→_{△}^{水}$HOCH2CH=CH2+NaCl | |
| D. | 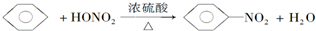 |
查看答案和解析>>
科目: 来源: 题型:解答题
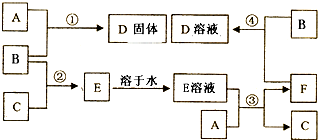
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
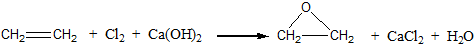
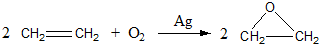
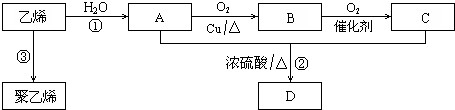
 ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目: 来源: 题型:填空题
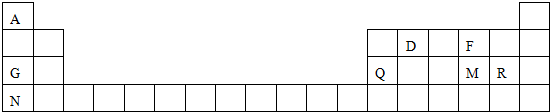
 .
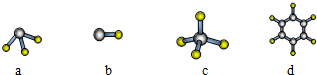
.
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙酸乙酯的制备实验中,用饱和氢氧化钠溶液来吸收随乙酸乙酯蒸出的少量乙酸和乙醇 | |
| B. | 甲烷跟氯气反应生成的CH3Cl、CH2Cl2、CHCl3、CCl4均为不溶于水的油状液体 | |
| C. | 石油的蒸馏,温度计的水银球必须插入反应液液面以下 | |
| D. | 水与金属钠反应比乙醇与金属钠反应更剧烈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com