
科目: 来源: 题型:选择题
 用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )
用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为( )| A. | 22.40 mL | B. | 22.30 mL | C. | 23.65 mL | D. | 23.70 mL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 沉淀溶解达到平衡时,沉淀的速率和溶解的速率相等 | |
| B. | 电解质的溶解开始后,只有电解质的溶解过程,没有电解质的析出过程 | |
| C. | 沉淀溶解达到平衡时,溶液中溶质的各离子浓度相等,且保持不变 | |
| D. | 沉淀溶解达到平衡时,如果再加入难溶性的该沉淀物,将促进溶解 |
查看答案和解析>>
科目: 来源: 题型:选择题
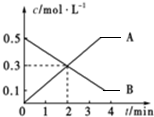
| A. | 前2 min内平均反应速率v(B)=0.3 mol•L-1•min-1 | |
| B. | 当A、B浓度不再变化时,此时反应速率为零 | |
| C. | 该反应的化学方程式为2A?3B | |
| D. | 前2 min内平均反应速率v(A)=0.15 mol•L-1•min-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | A>B | B. | A=10-10 B | C. | B=10-4 A | D. | A=B |
查看答案和解析>>
科目: 来源: 题型:选择题
 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示.下列叙述中不正确的是( )| A. | ROH是一种强碱 | B. | 在x点,MOH并没有完全电离 | ||
| C. | 在x点,c(M+)=c(R+) | D. | 稀释前,c(ROH)=10c(MOH) |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | ||
| CO(g) | H2O(g) | CO2(g) | H2(g) | ||
| ① | 430 | 1 | 1 | 0.95 | 0.95 |
| ② | 830 | 1 | 1 | 0.5 | 0.5 |
| ③ | 830 | 1.5 | 1 | ||
| A. | 正反应的△H>0 | B. | CO转化率③>② | ||
| C. | 实验①达到平衡的时间比②短 | D. | 430℃时,该反应的平衡常数为361 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
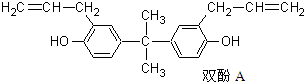
| A. | 该化合物的化学式为C20H24O2 | |
| B. | 该化合物与三氯化铁溶液反应显紫色 | |
| C. | 该化合物的所有碳原子处于同一平面 | |
| D. | 1mol双酚A最多可与4mol Br2发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com