
科目: 来源: 题型:解答题
 下表是某超市出售的加碘食盐的有关说明:
下表是某超市出售的加碘食盐的有关说明:| 配 料 表 | 精制盐、碘酸钾 |
| 含 碘 量 | 45±5mg/kg |
| 储 藏 方 法 | 通风、防潮 |
| 食 用 方 法 | 根据烹调所需适量加入 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 三者对应的氧化物均为碱性氧化物 | |
| B. | 三者的单质放置在空气中只生成氧化物 | |
| C. | 制备FeCl3不能采用将溶液直接蒸干的方法 | |
| D. | 电解AlCl3溶液是阴极上析出Al |
查看答案和解析>>
科目: 来源: 题型:选择题
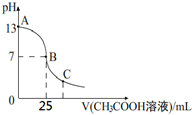 25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )| A. | A、B间的溶液中可能有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | B点:c(CH3COO-)=c(Na+)>c(OH-)=c(H+) | |
| C. | C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | NaOH溶液和醋酸溶液的浓度都恰好为0.1 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
 (1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-
(1)炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑.请回答:铁锅的锈蚀是吸氧腐蚀(填“析氢”或“吸氧”).写出铁锅腐蚀正极的电极反应式:2H2O+O2+4e-=4OH-查看答案和解析>>
科目: 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 次氯酸的电离方程式:HClO?H++ClO- | |
| B. | 铝溶于烧碱溶液的离子方程式:Al+2OH-═AlO2-+H2↑ | |
| C. | 电解精炼铜的阴极反应式:Cu-2e-═Cu2+ | |
| D. | 已知中和热为57.3 kJ•mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH (aq)═Na2SO4 (aq)+2H2O ( l )△H=+114.6 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 凡金属跟非金属元素化合时都能形成离子键 | |
| B. | 离子化合物熔融状态下一定导电 | |
| C. | 离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol 任何物质所含的分子数均为NA个 | |
| B. | 14 g氮气所含的N原子数为NA个 | |
| C. | 标准状况下,22.4 L水所含的H2O分子数为NA个 | |
| D. | 在钠与氯气的反应中,1 mol钠失去电子的数目为2 NA个 |
查看答案和解析>>
科目: 来源: 题型:选择题
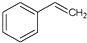 )的下列叙述,正确的是( )
)的下列叙述,正确的是( )| A. | 苯乙烯不可能发生加成反应 | |
| B. | 苯乙烯不可能使酸性高锰酸钾溶液褪色 | |
| C. | 苯乙烯不可能使溴的四氯化碳溶液褪色 | |
| D. | 苯乙烯可通过加聚反应生成高分子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com