
科目: 来源: 题型:解答题
| b | |||||||||||||||||
| h | j | ||||||||||||||||
| a | c | f | i | l | m | ||||||||||||
| e | g | ||||||||||||||||
| d | k | ||||||||||||||||
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.查看答案和解析>>
科目: 来源: 题型:解答题
| 分子或离子 | SO3 | SO2 | ClO3- | HCN | NF3 | NO3- |
| 中心原子孤电子对数 | 0 | 1 | 1 | 0 | 1 | 0 |
| σ键电子对数 | 3 | 2 | 3 | 2 | 3 | 3 |
| 中心原子的杂化轨道类型 | Sp2 | Sp2 | Sp3 | Sp | Sp3 | Sp2 |
| VSEPR模型名称 | 平面三角形 | V形 | 四面体 | 直线形 | 四面体 | 平面三角形 |
| 分子或离子立体构型名称 | 平面三角形 | V形 | 三角锥 | 直线形 | 三角锥 | 平面三角形 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2 | B. | C2H2 | C. | COCl2 | D. | H2O2 |
查看答案和解析>>
科目: 来源: 题型:解答题
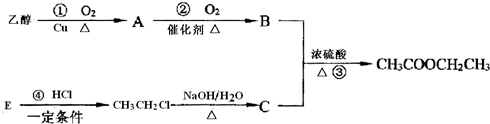
 CH3COOCH2CH3+H2O;④CH2=CH2+HCl
CH3COOCH2CH3+H2O;④CH2=CH2+HCl CH3CH2Cl.
CH3CH2Cl.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下端放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 蒸发结晶时应将溶液直接蒸干 | |
| D. | 称量非腐蚀性药品应放在托盘天平左盘的称量纸上,砝码放在托盘天平右盘的称量纸上 |
查看答案和解析>>
科目: 来源: 题型:解答题
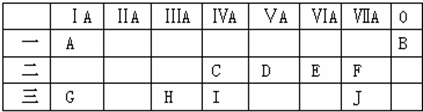
 ,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.
,元素H与元素J组成的化合物的水溶液中加入少量烧碱溶液,反应的离子方程式为Al3++3OH-=Al(OH)3↓.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com