
科目: 来源: 题型:选择题
| A. | 锂离子电池已成为笔记本电脑、移动电话等低功耗电器的主流电源 | |
| B. | 氢氧燃料电池可将化学反应的热能直接转变为电能 | |
| C. | 铅蓄电池放电时铅在负极被氧化成二氧化铅 | |
| D. | 锌锰干电池工作一段时间后碳棒变细 |
查看答案和解析>>
科目: 来源: 题型:解答题
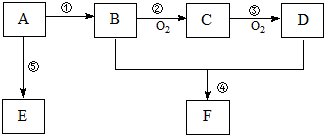
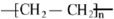 ,B中官能团的名称为羟基.
,B中官能团的名称为羟基. .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH≡CH | C. | CH2=CHCl | D. | CH≡CCH3 |
查看答案和解析>>
科目: 来源: 题型:解答题
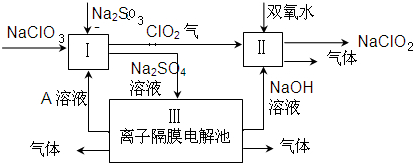
查看答案和解析>>
科目: 来源: 题型:解答题
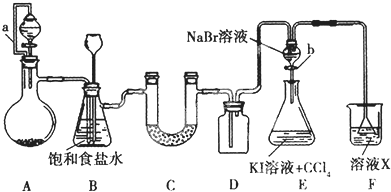
查看答案和解析>>
科目: 来源: 题型:解答题
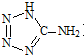 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 ;
;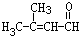 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com