
科目: 来源: 题型:选择题
| A. | 若再滴加KSCN溶液,溶液未变红,说明铁粉未变质 | |
| B. | 若再依次滴加氯水、KSCN溶液,溶液变红,说明铁粉部分变质 | |
| C. | 若再滴加KSCN溶液,溶液变红,说明铁粉部分变质或全部变质 | |
| D. | 若再滴加KSCN溶液,溶液未变红,再滴加氯水,溶液变红,说明铁粉全部变质 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 36g H2O中含有氧原子数为2NA | |
| B. | 标准状况下,11.2L苯所含分子数为0.5NA | |
| C. | 1L 1 mol•L-1硫酸钠溶液中,所含钠离子数为NA | |
| D. | 1mol H2在O2中完全燃烧转移的电子数目为NA |
查看答案和解析>>
科目: 来源: 题型:解答题
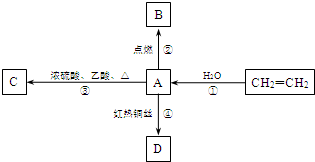 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种转化.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种转化. CH3COOCH2CH3+H2O,该反应的类型是:取代(或酯化)反应.
CH3COOCH2CH3+H2O,该反应的类型是:取代(或酯化)反应.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com