
科目: 来源: 题型:选择题
| A. | 元素 A、B 组成的化合物常温下一定呈气态 | |
| B. | 元素 D 的最高价氧化物对应的水化物不是两性化合物 | |
| C. | 元素 C 的最高价氧化物对应的水化物是弱碱 | |
| D. | 化合物 AE 与 CE 有相同类型的化学键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2与水反应生成硫酸 | |
| B. | 我国大气中SO2的主要来源是汽车排出的尾气 | |
| C. | SO2能漂白某些物质如品红溶液,说明它具有氧化性 | |
| D. | SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 离子半径大小:F->Na+>Mg2+ | B. | 金属性强弱:K>Mg>Ca | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 碱性强弱:LiOH>NaOH>KOH? |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子最外层的电子数随核电荷数的增加而增多 | |
| B. | 单质的氧化性随核电荷数的增加而增强 | |
| C. | 氢化物的稳定性随核电荷数的增加而减弱 | |
| D. | 非金属性随核电荷数的增加而增强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加酸性高锰酸钾溶液,振荡 | B. | 加NaOH溶液,加热 | ||
| C. | 加新制氢氧化铜悬浊液,加热 | D. | 加Na2CO3溶液,加热 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甘氨酸 | B. | 丙氨酸 | C. | 苯丙氨酸 | D. | 葡萄糖 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
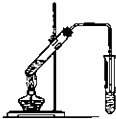 (1)某同学欲用12mol/L的浓盐酸配制1mol/L的盐酸250mL.
(1)某同学欲用12mol/L的浓盐酸配制1mol/L的盐酸250mL.查看答案和解析>>
科目: 来源: 题型:填空题
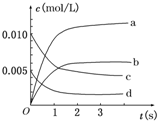 在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:
在2L密闭容器内,800℃时反应2SO2(g)+O2(g)?2SO3(g)体系中,n(SO2)随时间的变化如下表:| 时间 | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com