
科目: 来源: 题型:解答题
| 物质 | 加入试剂 | 操作方法 |
| ①苯(苯甲酸) | (2) | (4) |
| ②乙酸乙酯(乙醇) | (5) | (4) |
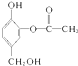 与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
与足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.查看答案和解析>>
科目: 来源: 题型:填空题
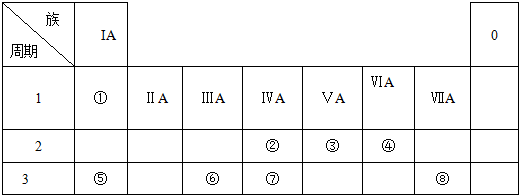
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
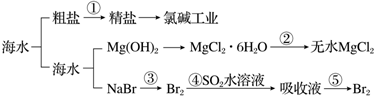
| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液-→NaOH溶液-→BaCl2溶液-→过滤后加盐酸 | |
| B. | 工业上金属钠是通过氯碱工业制取 | |
| C. | 从第③步到第⑤步的目的是为了富集溴元素 | |
| D. | 在第③④⑤步中溴元素均被氧化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑤⑥ | B. | ①②③④⑦ | C. | ③⑤⑥ | D. | ①③⑤⑥⑦ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑥ | C. | ①②④⑥ | D. | ②④⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:填空题
| 阳离子 | Na+、Al3+、Mg2+、Ba2+、Fe3+ |
| 阴离子 | Cl-、OH-、NO3-、CO32-、X |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2×10-2mol•L-1 | B. | 1×10-12mol•L-1 | C. | 1×10-2mol•L-1 | D. | 2×10-12mol•L-1. |
查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题
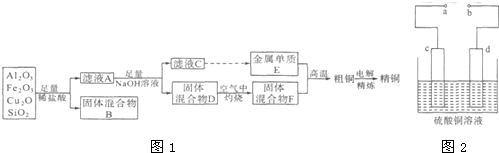
查看答案和解析>>
科目: 来源:2016-2017学年黑龙江大庆铁人中学高二上期中化学试卷(解析版) 题型:选择题
下列说法正确的一组是( )
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②盐都是强电解质
③弱酸、弱碱和水都是弱电解质
④强酸溶液的导电性一定强于弱酸溶液的导电性
⑤电解质溶液能导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电.
A.①③⑤⑥ B.②④⑤⑥ C.③⑤ D.③⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com