
科目: 来源: 题型:多选题
| A. | 1:3:5 | B. | 5:1:3 | C. | 3:1:5 | D. | 2:4:3 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 1mol O2和4mol NO2 | B. | 1mol NO和4mol NO2 | ||
| C. | 1mol O2和4mol NO | D. | 4mol NO和1mol NO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
 将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )
将一定量的Al2O3加入到100mL NaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0mol•L-1的盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是( )| A. | NaOH溶液的浓度为1.0mol•L-1 | |
| B. | Al2O3的质量为0.51g | |
| C. | v0的数值为35 | |
| D. | 沉淀量达到最大时,溶液中的溶质有两种 |
查看答案和解析>>
科目: 来源: 题型:填空题
 钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.
钇钡铜氧的晶胞结构如图.研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价.根据图示晶胞结构,推算晶体中Y、Ba、Cu和O原子个数比,确定其化学式为YBa2Cu3O7.查看答案和解析>>
科目: 来源: 题型:解答题
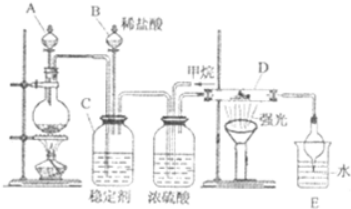 氯及其化合物在合成消毒剂、药物等方面具有广泛用途.二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,某兴趣小组通过如图装置,对二氧化氯及氯气的性质进行了研究:
氯及其化合物在合成消毒剂、药物等方面具有广泛用途.二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,某兴趣小组通过如图装置,对二氧化氯及氯气的性质进行了研究:查看答案和解析>>
科目: 来源: 题型:解答题

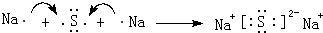 .
.查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 0-6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| B. | 6-10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min) | |
| C. | 反应到6min时,H2O2分解了50% | |
| D. | 反应到6min时,c(H2O2)=0.30mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com