
科目: 来源: 题型:选择题
| A. | 同一周期的非金属元素,由左到右其氧化物对应水化物的酸性依次递增 | |
| B. | aXn-与bYm+两种离子电子层结构相同,则b-a=n+m | |
| C. | 同一主族非金属元素对应氢化物稳定性依次递增,是由于其相对分子质量依次递增、分子间作用力增强所导致的 | |
| D. | 同一主族非金属元素对应氢化物沸点由上到下依次递增 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | ①、②、③互为同位素 | B. | ①、②、③互为同素异形体 | ||
| C. | ①、②、③是三种化学性质不同的核素 | D. | ①、②、③质量数相同 |
查看答案和解析>>
科目: 来源: 题型:解答题
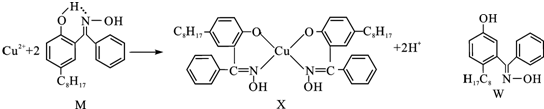
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
查看答案和解析>>
科目: 来源: 题型:解答题
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 位于周期表中第4纵行 |
| e | 基态原子M层全充满,N层只有一个电子 |
 .
. 、
、 、
、 、
、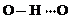 任意一种.
任意一种.查看答案和解析>>
科目: 来源: 题型:解答题
| a | |||||||||||||||||
| f | h | i | |||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | k | ||||||||||||||
| l | |||||||||||||||||
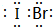 ,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).
,它是由δ键(根据原子轨道的重叠程度填写)形成的共价化合物(填“离子”或“共价”).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致 | |
| B. | 由于NaCl晶体和CsCl晶体中正负离子半径比不相等,所以两晶体中离子的配位数不相等 | |
| C. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| D. | MgO的熔点比MgCl2高主要是因为MgO的晶格能比MgCl2大 |
查看答案和解析>>
科目: 来源: 题型:解答题
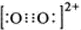 ; O22+中σ键数目和π键数目之比为1:2.
; O22+中σ键数目和π键数目之比为1:2.
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 负极反应为:O2+2H2O+4e═4OH- | |
| B. | 负极反应为:CH4+10OH--8e═CO32-+7H2O | |
| C. | 放电时溶液中的阳离子向负极移动 | |
| D. | 随放电的进行,溶液的pH值不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
 在2010年12月初农兴中学顺利接受省级示范高中验收期间,学校租用了大量盆栽鲜花装扮校园.为保证鲜花盛开,这些盆栽鲜花都施用了S-诱抗素剂,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
在2010年12月初农兴中学顺利接受省级示范高中验收期间,学校租用了大量盆栽鲜花装扮校园.为保证鲜花盛开,这些盆栽鲜花都施用了S-诱抗素剂,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A. | S-诱抗素含有苯环、羟基、羰基、羧基 | |
| B. | S-诱抗素能与NaHCO3反应放出CO2 | |
| C. | S-诱抗素的分子式为C14H20O4 | |
| D. | 1molS-诱抗素在一定条件下可分别与4molH2、2molNaOH发生反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com