
科目: 来源: 题型:选择题
| A. | 用加热分解的方法可区分碳酸钠和碳酸氢钠两种固体 | |
| B. | 向某溶液中加入过量的浓盐酸,有白色沉淀生成,该溶液中可能含SiO32- | |
| C. | 向某溶液中加入盐酸酸化的BaC12溶液,有白色沉淀生成,该溶液中一定含SO42- | |
| D. | 配制0.1000mol/L氢氧化钠溶液时,将液体转移到容量瓶中,需用玻璃棒引流 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,3.0g乙烷中含有的碳氢键数为0.7NA | |
| B. | 标准状况下,22.4L C2H5OH中含有的氢原子数为6NA | |
| C. | 常温常压下,92 g的 NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 标准状况下,由Na2O2制得11.2 LO2,反应转移的电子数为0.5NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 建立合法、公开的地沟油回收生产制度,将生产的地沟油用作工业用油 | |
| B. | 将生活垃圾分类回收,加工、使之再生、再利用 | |
| C. | 生活污水、工业废水不要乱排放,通过打深井,将之排到地层深处 | |
| D. | 不用一次性筷子、不浪费纸张、不浪费粮食、做“光盘”一族 |
查看答案和解析>>
科目: 来源: 题型:选择题
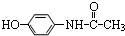 ,则有关它的性质错误的是( )
,则有关它的性质错误的是( )| A. | 与氢氧化钠溶液共热消耗2molNaOH | B. | 能与浓溴水发生取代反应 | ||
| C. | 不能使酸性高锰酸钾溶液褪色 | D. | 遇三氯化铁溶液呈现紫色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 条件 | 结论 |
| A | 若X原子半径X>Y | 原子序数:X<Y |
| B | 若最高价氧化物对应水化物酸性X>Y | 元素的电负性:X>Y |
| C | 若价电子数X>Y | 最高正价:X>Y |
| D | 若X、Y最外层电子数分别为1、7 | X、Y之间一定能形成离子键 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 它的原子核外电子共有16种不同的运动状态 | |
| B. | 它的原子核外有三种形状不同的电子云 | |
| C. | 它可与H2反应生成常温时的液态化合物 | |
| D. | 核外电子轨道表示式为: |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
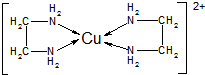
查看答案和解析>>
科目: 来源: 题型:解答题
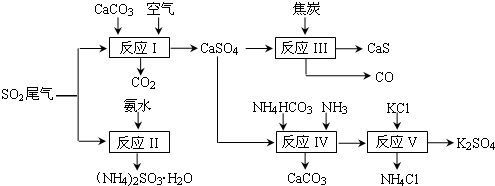
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com