
科目: 来源: 题型:选择题
| A. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| B. | 戊烷(C5H12)有两种同分异构体 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | 糖类、油脂和蛋白质均可发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 石油只含碳、氢两种元素,是多种烃的混合物 | |
| B. | 石油裂解得到的汽油是纯净物 | |
| C. | 石油是液态的物质,只含液态烃 | |
| D. | 石油的大部分是液态烃,其中溶有气态烃和固态烃 |
查看答案和解析>>
科目: 来源: 题型:解答题
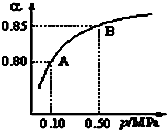
查看答案和解析>>
科目: 来源: 题型:解答题

| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 离子 | Cu2+ | Al3+ | NO3- | Cl- |
| 物质的量浓度(mol•L-1) | 1 | 0.1 | a | 1 |
| A. | 电解后溶液的pH=14 | B. | a=0.3 | ||
| C. | 阳极生成1.5 mol Cl2 | D. | 阴极滴加酚酞会变红 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.l mol•L-1醋酸钙溶液中,c(Ca2+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 等体积等pH的NH4Cl溶液、盐酸,完全溶解少量且等同的锌粉,前者用时少 | |
| C. | 将n mol H2(g)、n mol I2(g)和2n mol H2 (g)、2n mol I2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 | |
| D. | 某物质的溶液中由水电离出的c(H+)=1×10-a mol•L-1,若a>7时,则该溶液的pH一定为14-a |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氨水 | B. | 氢氧化钠 | C. | 碳酸钠 | D. | 碱式碳酸镁 |
查看答案和解析>>
科目: 来源: 题型:填空题
 人们对苯的认识有一个不断深化的过程.
人们对苯的认识有一个不断深化的过程.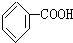 )和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与NaOH共热生成苯的化学方程式:
)和石灰的混合物得到液体,命名为苯,写出苯甲酸钠与NaOH共热生成苯的化学方程式: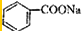 +NaOH$→_{△}^{氧化钙}$Na2CO3+
+NaOH$→_{△}^{氧化钙}$Na2CO3+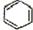 .
.
 )脱
)脱查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com