
科目: 来源: 题型:选择题
| A. | 苯、汽油、植物油和聚乙烯塑料都是碳氢化合物 | |
| B. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| C. | 水电站把机械能转化成电能,而核电站是把化学能转化成电能 | |
| D. | 糖类、油脂、蛋白质都是高分子化合物,都能发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
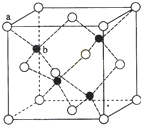 请完成下列各题:
请完成下列各题:查看答案和解析>>
科目: 来源: 题型:选择题
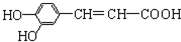 下列有关咖啡酸的说法中,不正确的是( )
下列有关咖啡酸的说法中,不正确的是( )| A. | 1mol咖啡酸可与3mol NaOH发生反应 | |
| B. | 咖啡酸可以发生还原、酯化、加聚、显色等反应 | |
| C. | 1mol咖啡酸可与4mol Br2发生反应 | |
| D. | 1mol咖啡酸最多可与5mol H2发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
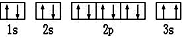 ,违背了泡利不相容泡利原理.
,违背了泡利不相容泡利原理.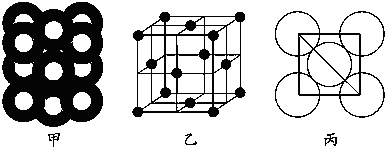
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6个120° | B. | 5个108° | C. | 4个109°28′ | D. | 6个109°28′ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 | |
| B. | 向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 | |
| C. | 将0.001 mol•L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 | |
| D. | 向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
查看答案和解析>>
科目: 来源: 题型:解答题
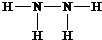 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com