
科目: 来源: 题型:选择题
| A. | 用新制的生石灰,通过加热蒸馏,可以除去乙醇中少量的水 | |
| B. | 用酸性高锰酸钾溶液,通过洗气的方法,可以除去甲烷中的乙烯 | |
| C. | 用苯,通过分液的方法,可以除去溴苯中的溴 | |
| D. | 用氢氧化钠溶液,通过分液的方法,可以除去乙酸乙酯中的乙酸 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | X试剂可用Na2SO3饱和溶液 | |
| B. | 步骤Ⅲ的离子反应:2Br-+Cl2═2Cl-+Br2 | |
| C. | 工业上每获得1molBr2,需要消耗Cl244.8L | |
| D. | 步骤Ⅳ包含萃取、分液和蒸馏 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 60g丙醇中存在的共价键总数为10 NA | |
| B. | 1L 0.1mol/L NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA | |
| C. | 钠在空气中可生成多种氧化物.23g钠充分燃烧时转移电子数为1 NA | |
| D. | 235g核素${\;}_{92}^{235}$U发生裂变反应:${\;}_{92}^{235}$U+${\;}_{0}^{1}$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{34}^{136}$Xe+10${\;}_{0}^{1}$n,净产生的中子(${\;}_{0}^{1}$n)数为10 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
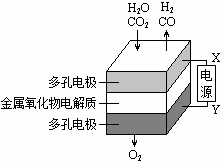 在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )
在固态金属氧化物电解池中,高温共电解H2O-CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )| A. | X是电源的负极 | |
| B. | 阴极的反应式是:H2O+2eˉ═H2+O2ˉ CO2+2eˉ=═CO+O2ˉ | |
| C. | 总反应可表示为:H2O+CO2$\frac{\underline{\;电解\;}}{\;}$H2+CO+O2 | |
| D. | 阴、阳两极生成的气体的物质的量之比是1:1 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 常温下,浓度均为0.1mol•L-1的四种溶液:
常温下,浓度均为0.1mol•L-1的四种溶液:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1mol/L pH=9的NaNO2溶液中C(Na+)>C(NO2-)>C(OH-)>C(H+) | |
| B. | 0.1mol/LNa2S溶液中:2C(Na+)=C(S2-)+C(HS-)+C(H2S) | |
| C. | 等PH的氨水、NaOH溶液、Ba(OH)2溶液中:C(NH4+)=C(Na+)=C(Ba2+) | |
| D. | 向NH4HCO3溶液中滴加NaOH溶液至pH=7:C(NH4+)+C(Na+)=C(HCO32-)+C(CO32-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X和Y可能都是固体 | B. | X和Y至少有一种是气体 | ||
| C. | X和Y可能都是气体 | D. | X和Y一定都是气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com