
科目: 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | 只有② | D. | 只有④ |
查看答案和解析>>
科目: 来源: 题型:选择题
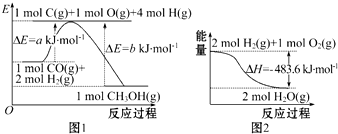
| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者△H小 | |
| C. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④⑥⑧⑩ | B. | ②③⑦⑧⑨ | C. | ②⑤⑨ | D. | ②⑥⑨ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 废电池需回收,主要是要利用电池外壳的金属材料 | |
| D. | 升高温度可降低活化能,增大反应速率 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 上述反应中NO2- 是氧化剂 | |
| B. | 反应过程中溶液的pH增大 | |
| C. | 该反应可以说明氧化性NO3->MnO4- | |
| D. | 上述反应中,1 mol KMnO4可以消耗2.5 mol NaNO2 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | Na与O2 | B. | NaOH与CO2 | C. | Na2O与CO2 | D. | Na2O2与H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 有2个A原子 | B. | 有2个氧原子 | C. | 有1个A原子 | D. | 有1个氧原子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用铝粉和MnO2制得锰 | |
| B. | 用电解熔融氯化铝的方法制得单质铝 | |
| C. | 氯化铝溶液和过量氢氧化钠溶液反应制备Al(OH)3 | |
| D. | 用镁粉和空气反应制备Mg3N2 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 实验Ⅰ:左边的棉球呈橙色,右边的棉球呈蓝色,证明氧化性:Cl2>Br2>I2 | |
| B. | 实验Ⅱ:当溶液至红褐色,停止加热,让光束通过体系时可产生丁达尔现象 | |
| C. | 实验Ⅲ:可通过铜丝的上下移动来控制NO2的制取并收集NO2气体 | |
| D. | 实验Ⅳ:振荡后静置,溶液不再分层,且保持无色透明 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com