
科目: 来源: 题型:选择题
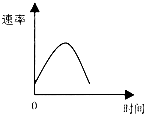 把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示.在下列因素中对产生H2速率有影响的是( )| A. | ①④ | B. | ③④ | C. | ①②③ | D. | ②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe、Zn | B. | Al、Cu | C. | Al、Fe | D. | Cu、Mg |
查看答案和解析>>
科目: 来源: 题型:解答题
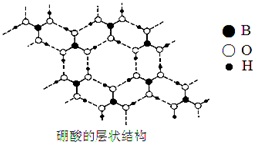 硼(B)及其化合物在化学中有重要的地位.请回答下列问题:
硼(B)及其化合物在化学中有重要的地位.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烯使溴水褪色,乙醇使酸性KMnO4溶液褪色,两者化学反应类型相同 | |
| B. | 1mol乙烯和Cl2完全加成后,再与Cl2彻底取代,两过程共消耗5mol Cl2 | |
| C. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 | |
| D. | 共价化合物中一定含有共价键,可能含有离子键 |
查看答案和解析>>
科目: 来源: 题型:选择题
 H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A. | 2c1>c3 | B. | a+b=92.4 | C. | 2p2<p3 | D. | α1+α2>1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 质量数是60 | B. | 质子数是27 | C. | 中子数是33 | D. | 电子数是33 |
查看答案和解析>>
科目: 来源: 题型:解答题
 周期表中前四周期的六种元素A、B、C、D、E、F的原子序数依次增大,已知A原子2p轨道有3个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D的单质晶体的熔点在同周期形成的单质中最高;F2+核外各亚层电子均已充满.
周期表中前四周期的六种元素A、B、C、D、E、F的原子序数依次增大,已知A原子2p轨道有3个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D的单质晶体的熔点在同周期形成的单质中最高;F2+核外各亚层电子均已充满.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com