
科目: 来源: 题型:多选题
| A. | 价电子排布为4s24p2的元素位于第四周期第ⅤA族,是P区元素 | |
| B. | 1,2-二甲苯核磁共振氢谱中有三组峰,且氢原子数之比为3:1:1 | |
| C. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 | |
| D. | 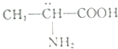 分子属于手性分子 分子属于手性分子 |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:多选题
| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 原子个数比 | B:A=1:3 | C:A=1:2 | D:A=1:1 | E:A=1:1 |
| A. | 元素E在元素周期表中的位置为第三周期、VIIA族 | |
| B. | 原子半径:A<B<C<D | |
| C. | 甲和丙分子均只含极性键 | |
| D. | A、B、C、D四种元素中的三种能形成多种与甲分子等电子数的化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素周期表中,电子层数越多,半径一定越大 | |
| B. | 元素周期表中,同一主族,随着核电荷数的递增,熔沸点逐渐降低 | |
| C. | 非金属元素与非金属元素之间可能形成离子键 | |
| D. | 含有离子键的物质一定是离子化合物,只含共价键的物质一定是共价化合物 |
查看答案和解析>>
科目: 来源: 题型:解答题
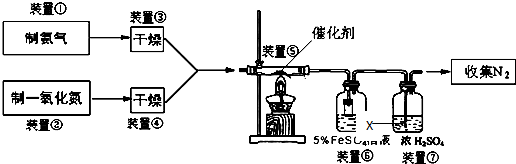

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH3CH2OH 和CH3OCH3 | B. | 淀粉和纤维素 | ||
| C. | 金刚石和石墨 | D. | CH3CH2CH3和CH3CH2CH2CH3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢氧化钡溶液与稀硫酸反应:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O | |
| B. | 铁与稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | 用FeCl3溶液腐蚀电路板上多余的铜:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 碳酸氢钠溶液与稀盐酸反应:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量氧气中完全燃烧转移的电子数为2NA | |
| D. | 28g N2中含有的原子数为2NA |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com