
科目: 来源: 题型:选择题
| A. | 过氧化钠、纯碱分别属于碱性氧化物、碱 | |
| B. | NO、NO2 都是大气污染物,在空气中都能稳定存在 | |
| C. | SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 | |
| D. | 检验某浅绿色溶液中含有Fe2+:取该溶液少许,向其中加入KSCN溶液,不变红色,再向其中滴加氯水,溶液变为红色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 44gCO2 的体积为22.4L | |
| B. | 标准状况下,22.4L水中含有NA个水分子 | |
| C. | 常温常压下,28gN2中所含的原子数目为2NA | |
| D. | 如果11.2LN2中含有n个氮气分子,则阿佛加德罗常数一定为2n |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题


 (R1、R2、R3为烃基或氢原子)
(R1、R2、R3为烃基或氢原子) .
. .
.查看答案和解析>>
科目: 来源: 题型:解答题
 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.| 元素 | Mn | Fe | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目: 来源: 题型:解答题
| 时间(h) | 1 | 2 | 3 | 4 | 5 | 6 |
| P后/P前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
查看答案和解析>>
科目: 来源: 题型:解答题
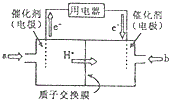 二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空:
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或H2SO4反应生成SeO2以回收Se.完成下列填空:查看答案和解析>>
科目: 来源: 题型:选择题
 苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )
苹果iphone6正在我国热卖,其电池为锂电池.构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6$?_{放电}^{充电}$LiCoO2+6C,下列说法错误的是( )| A. | 该电池放电时的负极材料为LiCoO2 | |
| B. | 电池中的固体电解质可以是熔融的氯化钠、氯化铝等 | |
| C. | 充电时的阴极反应:Li1-xCoO2+xLi++xe-═LiCoO2 | |
| D. | 外电路上的“→”表示放电时的电子流向 |
查看答案和解析>>
科目: 来源: 题型:解答题
 能源的发展日益成为全世界、全人类共同关心的问题.
能源的发展日益成为全世界、全人类共同关心的问题.| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899 | 1 757 | 14 840 | 21 000 |
| B | 738 | 1 451 | 7 733 | 10 540 |
查看答案和解析>>
科目: 来源: 题型:解答题
 决定物质性质的重要因素是物质的结构.请回答下列问题:
决定物质性质的重要因素是物质的结构.请回答下列问题:| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1 817 | 2 745 | 11 578 |
| B | 738 | 1 451 | 7 733 | 10 540 |
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com