
科目: 来源: 题型:选择题
| A. | vA=0.5mol/(L•s) | B. | vB=0.2mol/(L•s) | C. | vC=0.9mol/(L•s) | D. | vD=1.1mol/(L•s) |
查看答案和解析>>
科目: 来源: 题型:解答题
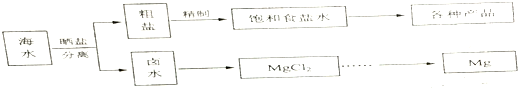
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.6 |
| Mg(OH)2 | 9.8 | 11.1 |
查看答案和解析>>
科目: 来源: 题型:解答题
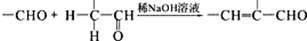 ;
; 
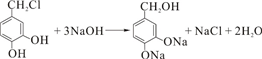 .
.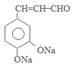 +2Ag(NH3)2OH$\stackrel{水浴}{→}$
+2Ag(NH3)2OH$\stackrel{水浴}{→}$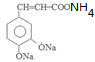 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.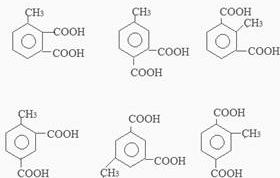 (任三种).
(任三种).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| B. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA | |
| B. | 1 L 1 mol•L-1 NH4NO3溶液中氮原子数小于2NA | |
| C. | 常温常压下,11.2 g乙烯中含有共用电子对数目为2.4NA | |
| D. | 标准状况下,22.4 L CHCl3中所含有的分子数为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 食盐和油都是生活必需品.加碘盐中的碘以碘化钾的形式存在;而植物油变质是由于发生了酯化反应 | |
| B. | “神十”搭载的长二F改进型火箭推进剂是偏二甲肼(C2H8N2)和四氧化二氮,其中四氧化二氮作氧化剂 | |
| C. | 镁铝合金可用作制造飞机的材料 | |
| D. | 近期正热播柴静的雾霾调查纪录片《穹顶之下》.PM2.5是灰霾天气的主要原因,是指大气中直径小于或等于2.5微米的颗粒物,也叫可入肺颗粒物,与肺癌、哮喘等疾病的发生密切相关,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
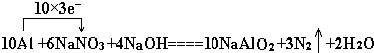
查看答案和解析>>
科目: 来源: 题型:解答题
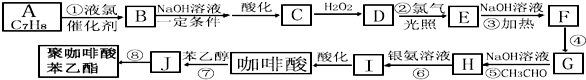
 是一种环保型的新涂料,其合成路线如图所示:请回答下列问题:
是一种环保型的新涂料,其合成路线如图所示:请回答下列问题:
 .
. .
. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式). CH2CH=CH2合成B的另一种途径为:
CH2CH=CH2合成B的另一种途径为: CH2CH=CH2$\stackrel{Cl_{2}+CCl_{4}}{→}$F$→_{△}^{NaOH溶液}$H$\stackrel{氧化}{→}$
CH2CH=CH2$\stackrel{Cl_{2}+CCl_{4}}{→}$F$→_{△}^{NaOH溶液}$H$\stackrel{氧化}{→}$ $→_{一定条件}^{G}$
$→_{一定条件}^{G}$ ,试剂G的化学式H2.
,试剂G的化学式H2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com