
科目: 来源: 题型:选择题

| A. | 该过程是一种新的硫酸生产方法 | |
| B. | C2H5OSO3H具有酸性 | |
| C. | 该过程中①、②是加成反应 | |
| D. | 该过程中③、④可看做酯类的水解反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2 mol SO2+1 mol O2 | B. | 4 mol SO2+1 mol O2 | ||
| C. | 2 mol SO2+1 mol O2+2 SO3 | D. | 3 mol SO2+1 SO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
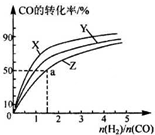 天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.
天然气、可燃冰的主要成分都是甲烷,甲烷既是一种清洁能源,又是一种重要的化工原料.| 温度(℃) | 800 | 1000 | 1200 | 1400 |
| 平衡常数(K) | 0.45 | 1.92 | 276.5 | 1771.5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 弱酸 | HA | HB | H2C |
| 电离平衡常数 (25℃) | K1=1.77×10-4 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | B-+HA→HB+A- | |
| B. | 2Bˉ+H2C→2HB+C2- | |
| C. | 中和等体积、等pH的HA和HB消耗NaOH的量前者小于后者 | |
| D. | 等体积、等浓度的NaA和NaB溶液中所含离子总数前者大于后者 |
查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe2O3•2SO3•7H2O | B. | 4Fe2O3•10SO3•25H2O | ||
| C. | 3Fe2O3•6SO3•20H2O | D. | 2Fe2O3•5SO3•17H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  用如图装置制取Fe(OH)2沉淀 | |
| B. |  用如图装置吸收NH3,并防止倒吸 | |
| C. |  用如图装置蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. |  用如图装置比较Na2CO2与NaHCO3的稳定性 |
查看答案和解析>>
科目: 来源: 题型:选择题
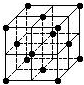
| A. | C60摩尔质量是720 | |
| B. | C60属于离子晶体 | |
| C. | 在C60晶胞中有14个C60分子 | |
| D. | 每个C60分子周围与它距离最近等距离的C60分子有12个 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com