
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6W% | B. | 3W% | C. | 大于3W% | D. | 小于3W% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 摩尔是国际单位制的一个基本物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 | |
| D. | 表示6.02×1023个粒子的集合体 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
查看答案和解析>>
科目: 来源: 题型:选择题
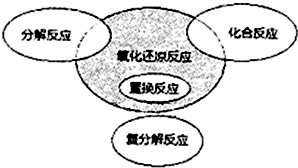
| A. | Cl2+2NaBr═2NaCl+Br2 | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ | D. | 4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba2+、NO3-、OH-、K+ | B. | H+、K+、CO32-、SO42- | ||
| C. | Mg2+、NH4+、OH-、Cl- | D. | Ba+、Na+、Cl-、SO42- |
查看答案和解析>>
科目: 来源: 题型:填空题
 将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.
将E单质缓慢通入石灰水中,若生成物中有三种含E元素的离子,其中两种离子的物质的量与反应时间的曲线如图所示,则t1时刻[n(EO-)=0.15mol]消耗氢氧化钙的物质的量为0.15mol,t2时总反应的化学方程式为10Cl2+10Ca(OH)2=7CaCl2+2Ca(ClO)2+Ca(ClO3)2+10H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com