
科目: 来源: 题型:选择题
| A. | 2Q2=Q1 | B. | 2Q2<Q1 | C. | Q2<Q1<197kJ | D. | Q2=Q1<197kJ |
查看答案和解析>>
科目: 来源: 题型:解答题
 HSO3-+OH-.
HSO3-+OH-.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 25℃时,1L pH=13的Ba(OH)2溶液中含OH-数目为0.2NA | |
| C. | 1L 1mol•L-1的Na2CO3溶液中含有CO32-的数目为NA | |
| D. | 18g H2O中含1mol氧原子 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol氧的质量为32g | |
| B. | 标准状况下,0.5 mol NO和0.5 mol O2的混合气体体积约为22.4L | |
| C. | CO2的摩尔质量为44g/mol | |
| D. | 1L 2 mol/L的BaCl2溶液中含Cl-的个数为2.408×1024 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①②④ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
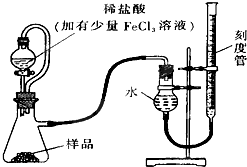 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量•
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量•
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com