
科目: 来源: 题型:解答题
 、醛基-CHO、羧基-COOH、-COOR酯基.
、醛基-CHO、羧基-COOH、-COOR酯基.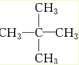 ,名称为2,2-二甲基丙烷.
,名称为2,2-二甲基丙烷.查看答案和解析>>
科目: 来源: 题型:解答题
 ,名称为2,2-二甲基丙烷(新戊烷).
,名称为2,2-二甲基丙烷(新戊烷).
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
| 实验操作 | 答案 | 实验现象 |
| (1)将浓硫酸滴在小木条上 | A.产生白烟 B.产生蓝色物质 C.溶液呈红色 D.变黑色 | |
| (2)将分别蘸浓氨水和浓盐酸的玻璃棒靠近 | ||
| (3)在盛有KI淀粉溶液的试管中滴加氯水 | ||
| (4)在盛有FeC13溶液的试管中滴入2滴KSCN溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ||||||
| 3 | ② | ③ | ④ | ⑥ |
 ;
;查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 氢氧化铝与盐酸:Al(OH)3+3H+═Al3++3H2O | |
| C. | 铁溶于氯化铁溶液:Fe+Fe3+═2Fe2+ | |
| D. | 氨气溶于醋酸:H++NH3═NH4+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应达到平衡时,降低温度,平衡逆向移动 | |
| B. | 使用催化剂,正反应速率增大,逆反应速率减小 | |
| C. | 加压,平衡不移动,但正、逆反应速率都不改变 | |
| D. | 减小SO2的浓度,平衡逆向移动 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com