
科目: 来源: 题型:选择题
| A. | 许多金属和合金具有低温下失去电阻的特性,即具有超导性 | |
| B. | 两个较轻的原子核聚合为一个较重的原子核时要释放出大量的能量,所释放的能量可用于发电 | |
| C. | 天然的、人为的各种电磁波干扰和有害的电磁辐射会造成电磁污染 | |
| D. | 美国科学家利用分子组装技术研制出世界上最小的“纳米算盘”,该算盘的算珠由球形C60分子构成 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 0.1mol•L-1氨水中,c(OH-)=c(NH4+) | |
| B. | 10 mL 0.02mol•L-1HCl溶液与10 mL 0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 | |
| C. | 在0.1mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| D. | 0.1mol•L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②⑤ | B. | ③⑤⑥ | C. | ②④ | D. | ②④⑥ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | CH3OH | B. | C3H8 | C. | C2H4 | D. | CH4 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 有机物 | 氢氧化钠 | 银氨溶液 | 新制氢氧化铜 | 金属钠 |
| A | 发生中和反应 | 不反应 | 溶解 | 放出氢气 |
| B | 不反应 | 发生银镜反应 | 生成红色沉淀 | 放出氢气 |
| C | 发生水解反应 | 发生银镜反应 | 生成红色沉淀 | 不反应 |
| D | 发生水解反应 | 不反应 | 不反应 | 不反应 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
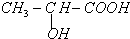 现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
现以A为主要原料合成乙酸乙酯,其合成路线如图所示.
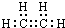 A结构式CH2=CH2
A结构式CH2=CH2查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com