
科目: 来源: 题型:解答题
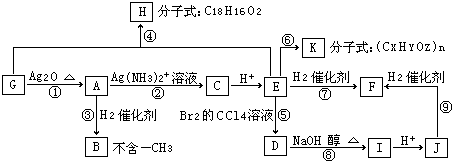
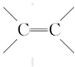 .
.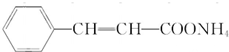 .物质K的结构简式
.物质K的结构简式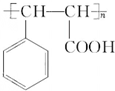 .
.

查看答案和解析>>
科目: 来源: 题型:解答题
 ,ZO3-的空间构型是平面三角形;
,ZO3-的空间构型是平面三角形;查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 ,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-).
,比较S2-与Cl-的半径大小:r(S2-)>(填“>”或“<”)r(Cl-).查看答案和解析>>
科目: 来源: 题型:解答题
| 活性炭(mol) | NO(mol) | CO2(mol) | N2(mol) | |
| 起始状态 | 3.0 | 0.8 | 0 | 0 |
| 2min时 | 2.8 | 0.4 | 0.2 | 0.2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氨水能导电,说明NH3是电解质 | |
| B. | 加水稀释,溶液中的c(OH-)增大 | |
| C. | 加入稀硫酸至溶液的pH=7,c(NH4+)=c(SO42-) | |
| D. | 向含有酚酞的氨水中加入少量NH4Cl晶体,溶液颜色变浅 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④⑦ | B. | ①③⑥ | C. | ③④⑤⑦ | D. | ②④⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯化铜溶液与铁粉反应:Cu2++Fe═Fe2++Cu | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下6.72 L CO | B. | 0.3NA个Na2SO3 | ||
| C. | 常温常压下9.6g O2 | D. | 1.806×1023个H2O分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com