
科目: 来源: 题型:解答题
 某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.
某课外兴趣小组进行了中和热测定实验,据此回答下列问题:用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.查看答案和解析>>
科目: 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目: 来源: 题型:解答题

 这个结构不稳定,自动脱水,生成碳基.
这个结构不稳定,自动脱水,生成碳基. ;有机物C的系统名称为:2-甲基丙醛.
;有机物C的系统名称为:2-甲基丙醛. .
.查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
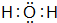 、
、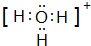 ;
;查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 18gD2O(重水)含有的质子数、电子数和中子数均为10NA | |
| B. | 2molSO2和1molO2通入密闭容器中,发生反应2SO2(g)+O2(g)$\frac{\underline{\;催化剂\;}}{△}$2SO3(g),反应完成时,生成SO3分子数小于2NA | |
| C. | 7.8gNa2O2固体含有的离子数为0.4NA | |
| D. | 2.24LH2完全燃烧时,断裂H-H键数目为0.1NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2=CH-CH3 | B. | CH2=CH-CH2-CH3 | ||
| C. | CH3=CH-CH2-CH=CH2 | D. | CH2=CH-CH2-CH2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 随着碳原子数的增加,烷烃的熔、沸点升高 | |
| B. | 在有机物中,碳原子通过四个共价键与其它原子结合 | |
| C. | 甲烷、乙烯都能使酸性高锰酸钾溶液褪色 | |
| D. | 烷烃在光照下与氯气发生取代反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com