
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

| 实验编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准 溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 解释或实验结论 |
| (1)取9.0g有机物A加热使其气化,测得其密度是相同条件下H2的45倍 | (1)由此可知A的相对分子质量为90. |
| (2)将9.0gA在足量O2中充分燃烧,其产物依次缓缓通过浓硫酸、碱石灰,两者分别增重5.4g和13.2g. | (2)由此可知A的分子式为C3H6O3. |
| (3)另取A9.0g,跟足量的NaHCO3粉末反应,生成CO2气体2.24L;9.0gA若与足量金属钠反应生成H2也是2.24L(气体体积皆为标准状况下测得). | (3)由此可知A中含有官能团有.(填结构简式)-COOH、-OH |
(4)A的核磁共振氢谱如下图: | (4)由此可知A中含有4种不同性质的氢原子 (5)综上,A的结构简式为  . . |
查看答案和解析>>
科目: 来源: 题型:解答题
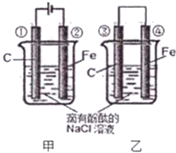 化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 $?_{暗处}^{光照}$
$?_{暗处}^{光照}$ △H=+88.6kJ•mol-1
△H=+88.6kJ•mol-1查看答案和解析>>
科目: 来源: 题型:多选题
 2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )
2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,该反应过程能量变化如图所示,下列叙述中正确的是( )| A. | 该反应的反应物总能量小于生成物总能量 | |
| B. | 该反应的逆反应为吸热反应 | |
| C. | 图中△H=-99kJ•mol-1, | |
| D. | 图中字母E所示能量值表示该反应的活化能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com