
科目: 来源: 题型:选择题
| A. | Na2S Na2O Na2SO3 | B. | Na2SO4Na2O Na2SO3 | ||
| C. | Na2O Na2S Na2SO4 | D. | Na2S Na2SO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
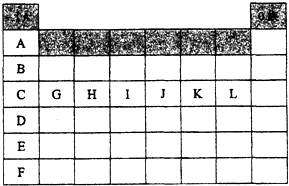 如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)
如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 黄铜属于合金,硬度比纯铜高 | |
| B. | MgO、Al2O3是耐高温材料,工业上常用其电解冶炼对应的金属 | |
| C. | 与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 | |
| D. | 金属单质与盐溶液的反应都是置换反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 增加N2的量,可以加快反应速率 | |
| B. | 当N2和H2全部转化为NH3时,反应才达到最大限度 | |
| C. | 达到平衡时,H2和NH3的浓度比一定为3:2 | |
| D. | 分别用N2和NH3来表示该反应的速率时,数值大小相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCl气体溶于水形成盐酸,存在H+,所以HCl为离子化合物 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 稀有气体原子之间不易形成共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 达平衡时,A2的正反应速率与B2的逆反应速率相等 | |
| B. | b≤0.2mol/L | |
| C. | 其它条件不变,在反应过程中使用了催化剂,可提高 A2、B2的转化率 | |
| D. | 该反应达平衡时气体物质的量浓度之和小于(a+b+0.3)mol/L |
查看答案和解析>>
科目: 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅤⅡA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,元素②原子核内含有6个中子的原子可表示为137N.
,元素②原子核内含有6个中子的原子可表示为137N. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com