
科目: 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②③⑤⑥⑦ | C. | ①②④⑤ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4 L氦气和1 mol氟气所含原子数均为2NA | |
| B. | 1 mol H2O、1 mol NH3 和1mo l OH-所含电子数均为10NA | |
| C. | 1 mol Na2O2与CO2反应电子转移为2NA | |
| D. | 标准状况下22.4L的氯气和某些物质反应,电子转移一定为2NA |
查看答案和解析>>
科目: 来源: 题型:解答题
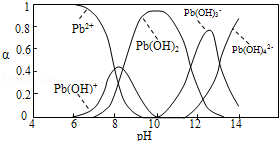
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度/(mg•L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度/(mg•L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
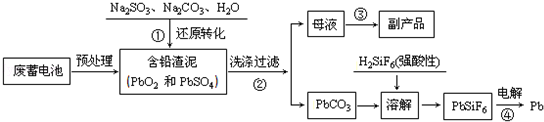
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
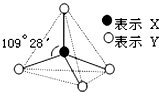 甲、乙、丙、丁、戊具有如图所示的结构或结构单元,图中四面体外可能有的部分未画出,只有实线表示共价键,X、Y可同可不同.
甲、乙、丙、丁、戊具有如图所示的结构或结构单元,图中四面体外可能有的部分未画出,只有实线表示共价键,X、Y可同可不同.查看答案和解析>>
科目: 来源: 题型:解答题
| Ⅰ实验结果 | Ⅱ回答问题 |
| ①取原溶液少许,滴加足量氯水,产生沉淀;过滤,滤液加CCl4,振荡后,CCl4层未变色. | ①该步实验说明溶液中不存在Br-离子I-. |
| ②取原溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色. | ②该步实验发生反应的离子方程式为 8H++2NO3-(稀)+3Cu=3Cu2++2NO↑+4H2O. |
| ③取原溶液少许,加盐酸酸化后,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失. | ③产生白色沉淀的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+. |
| ④取原溶液少许,滴加2滴酸性高锰酸钾溶液,紫色立即褪去. | ④该步实验说明溶液中存在SO32-离子. |
| ⑤取原溶液少许,加足量Ba(NO3)2溶液产生白色沉淀,过滤;往洗涤后的沉淀中加入足量盐酸,沉淀部分溶解,有无色气体产生. | ⑤未溶解的白色沉淀是BaSO4;将气体通入品红溶液的现象是品红溶液褪色. |
| ⑥取步骤⑤所得滤液,加HNO3酸化后,再加AgNO3溶液,溶液中析出白色沉淀. | ⑥该步骤是否有意义有(填“有”或“无”). |
查看答案和解析>>
科目: 来源: 题型:解答题
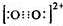 .CaC2晶胞结构与氯化钠晶体相似,则在晶体中与钙离子距离最近的C22-数目为6,这些C22-在空间所围成的几何图形为正八面体
.CaC2晶胞结构与氯化钠晶体相似,则在晶体中与钙离子距离最近的C22-数目为6,这些C22-在空间所围成的几何图形为正八面体查看答案和解析>>
科目: 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、Cl-、OH-、SO42- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com