
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻĖĪ¬ĖŲ±»ČĖĢåĻū»ÆĪüŹÕŗóĢį¹©ÓŖŃųĪļÖŹ | |
| B£® | ÄÜ·¢ÉśĖ®½ā·“Ó¦µÄ²»Ņ»¶ØŹĒĢĒĄą£¬µ«ĢĒĄąŅ»¶ØÄÜ·¢ÉśĖ®½ā·“Ó¦ | |
| C£® | ƻӊ³ÉŹģµÄĘ»¹ūÖÓöµā±äĄ¶É«£¬³ÉŹģµÄĘ»¹ūÖÄÜ»¹ŌŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ | |
| D£® | 1 mol¶žĢĒĶźČ«Ė®½āŅ»¶ØÄܹ»Éś³É2 molĘĻĢŃĢĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3øö | B£® | 4øö | C£® | 5øö | D£® | 6øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
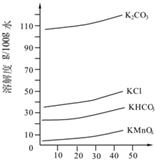 ŹµŃéŹŅÓĆMnO2”¢KOH¼°KClO3ĪŖŌĮĻÖĘČ”øßĆĢĖį¼ŲµÄŹµŃéĮ÷³ĢČēĻĀ£ŗ
ŹµŃéŹŅÓĆMnO2”¢KOH¼°KClO3ĪŖŌĮĻÖĘČ”øßĆĢĖį¼ŲµÄŹµŃéĮ÷³ĢČēĻĀ£ŗ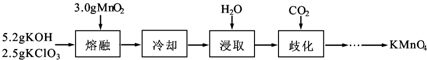
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į½ÖÖĪļÖŹµÄ×é³ÉŌŖĖŲĻąĶ¬£¬ø÷ŌŖĖŲµÄÖŹĮæ·ÖŹżŅ²ĻąĶ¬£¬ŌņĮ½ÕßŅ»¶Ø»„ĪŖĶ¬·ÖŅģ¹¹Ģå | |
| B£® | ·Ö×ÓŹ½ĪŖCnH2nµÄ»ÆŗĻĪļ£¬æÉÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬Ņ²æÉÄܲ»Ź¹ĘäĶŹÉ« | |
| C£® | ĶØŹ½ĻąĶ¬£¬·Ö×Ó×é³ÉÉĻĻą²īŅ»øö»ņČōøÉøöCH2Ō×ÓĶŵĻÆŗĻĪļ£¬Ņ»¶Ø»„ĪŖĶ¬ĻµĪļ | |
| D£® | ·²ŗ¬ÓŠ±½»·µÄĪļÖŹ¶¼ŹĒ·¼ĻćĢž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

 £¬
£¬ £¬
£¬ £»
£» £¬
£¬ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3ČÜŅŗ¼ÓĖ®Ļ”ŹĶŗ󣬻Öø“ÖĮŌĪĀ¶Č£¬ĖłÓŠĄė×ÓÅØ¶Č¾ł¼õŠ” | |
| B£® | pH=5µÄCH3COOHČÜŅŗŗĶpH=5µÄNH4ClČÜŅŗÖŠ£¬c£ØH+£©ĻąµČ | |
| C£® | pH=12µÄBa£ØOH£©2ČÜŅŗŗĶpH=12µÄNa2CO3ČÜŅŗÖŠ£¬Ė®µēĄėµÄc£ØH+£©Ē°Õß“ó | |
| D£® | 0.1mol•L-1CH3COONaČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØH+£©£¾c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com