
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
 :下列有关该化合物的说法中正确的是( )
:下列有关该化合物的说法中正确的是( )| A. | 分子式为C12H8O2Cl4 | B. | 是一种可溶于水的气体 | ||
| C. | 是最危险的致癌物之一 | D. | 是一种多卤代烃 |
查看答案和解析>>
科目: 来源: 题型:解答题
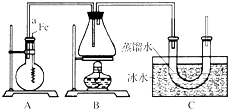 按如图所示的装置和以下实验步骤,可以制取少量的溴苯和溴乙烷.已知乙醇在一定条件下与氢溴酸反应可制备溴乙烷:
按如图所示的装置和以下实验步骤,可以制取少量的溴苯和溴乙烷.已知乙醇在一定条件下与氢溴酸反应可制备溴乙烷:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该装置能将电能转化为化学能 | B. | 实验过程中铜片逐渐溶解 | ||
| C. | 铁片上会析出红色的铜 | D. | 电子由铁片通过导线流向铜片 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 19种 | B. | 10种 | C. | 16种 | D. | 12种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 石油经过分馏及裂化等方法得到的物质均为纯净物 | |
| B. | 乙酸乙酯、油脂、葡萄糖、蛋白质均可以发生水解反应 | |
| C. | 化合物 是苯的同系物 是苯的同系物 | |
| D. | 地沟油和矿物油可通过加足量的氢氧化钠溶液加热后的不同现象加以区别 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应的水化物的酸性比W的强 | |
| D. | W的单质可用于制造光导纤维 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 三种元素的原子半径大小为X>Y>Z | B. | Y2-与Z+的半径大小为Y2->Z+ | ||
| C. | Y元素为S | D. | Z 元素为K |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com