
科目: 来源: 题型:解答题
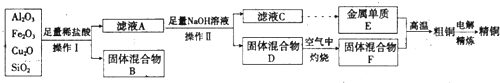
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在Na2S溶液中滴入酚酞试液,呈红色 | |
| B. | 升高温度能使FeCl3溶液中的H+浓度增大 | |
| C. | 一切钾盐、钠盐、硝酸盐都不发生水解 | |
| D. | 醋酸盐溶于水能发生水解 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 锌片逐渐溶解 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 电解质溶液的pH保持不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al3+Na+HCO3- Cl- | B. | K+ Na+ HCO3-AlO2- | ||
| C. | Mg2+ NH4+ SO42-Cl- | D. | Fe2+ Na+Cl- NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液的pH=4 | |
| B. | 适当升高温度,溶液的pH不变 | |
| C. | 此酸的电离平衡常数约为1×10-7 | |
| D. | 由HX电离出的c(H+)约为水电离出的c(OH-)的106倍 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硫化亚铁中加入盐酸:S2-+2H+═H2S↑ | |
| B. | 向Ca(ClO)2溶液中通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 硫酸铝溶液和少量苏打溶液反应:3H2O+Al3++3CO32-═3HCO3-+Al(OH)3↓ | |
| D. | 钠和冷水反应:2Na+2H2O═2Na++H2↑+2OH- |
查看答案和解析>>
科目: 来源: 题型:解答题
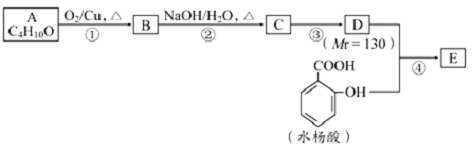
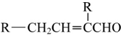 ;
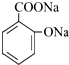
; 、-CHO;③的反应类型为加成反应(或还原反应).
、-CHO;③的反应类型为加成反应(或还原反应).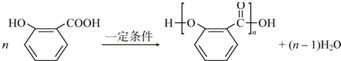 .
.
查看答案和解析>>
科目: 来源: 题型:解答题
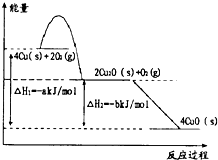 铜及其化合物在工业、农业、科技和日常生活中有广泛应用.
铜及其化合物在工业、农业、科技和日常生活中有广泛应用.查看答案和解析>>
科目: 来源: 题型:解答题
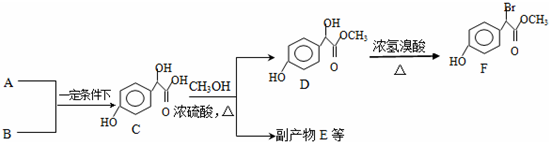
 .
.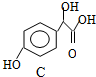 中①、②、③(从左到右编号)3个-OH的酸性由强到弱的顺序是:③>①>②.
中①、②、③(从左到右编号)3个-OH的酸性由强到弱的顺序是:③>①>②. .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com