
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
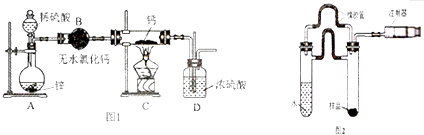
 实验室可用如图装置制取少量NaHSO3
实验室可用如图装置制取少量NaHSO3| 实验操作 | 预期现象与结论 |
步骤一、取少量待测液放入试管中,滴加过量lmol/L氯化钡溶液,静置 | 若产生白色沉淀(或浑浊)(填实验现象), 则产物中存在Na2SO3,否则无该物质. |
步骤二、取步骤一所得的上层澄清溶液少许与试管中,向其中加入过量lmol/L氢氧化钡溶液 | 若产生若产生白色沉淀(或浑浊)(填实验现象),则产物中存在NaHSO3,否则无该物质. |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

| 实验编号 | T/K | 反应时间/h | 反应物的物质的量配比n[CO(NH2)2]:n[MgCl2.6H2O] | 实验目的 |
| ① | 378 | 3 | 3:1 | (I)实验①和③探究反应物的物质的量配比对产率的影响 (II)实验②和④探究温度对产率的影响 (III)实验②和③探究反应时间对产率的影响 |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |

查看答案和解析>>
科目: 来源: 题型:解答题


| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com