
科目: 来源: 题型:选择题

| A. | 根据图1可知合成甲醇的热化学方程式为CO(g)+2H2(g)═CH3OH(g)△H1=(b-a)kJ•mol-1 | |
| B. | 图2表示2 mol H2(g)所具有的能量比2 mol气态水所具有的能量多483.6 kJ | |
| C. | 1 mol NaOH分别和1 mol 稀硫酸、1 mol浓硫酸反应,前者的△H比后者的△H大 | |
| D. | 汽油燃烧时将全部的化学能转化为热能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 钢铁在潮湿的空气中容易生锈 | |
| B. | 降低盐酸浓度以减缓盐酸与Zn反应的速率 | |
| C. | SO2氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 恒温恒压的容器中有2NO2?N2O4,若通入Ar,气体的颜色先变浅后逐渐加深 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用25mL量筒量取12.36mL盐酸 | |
| B. | 用托盘天平称量8.75g食盐 | |
| C. | 用广泛pH试纸测得某溶液的pH为3.5 | |
| D. | 配制240mL溶液选用250mL的容量瓶 |
查看答案和解析>>
科目: 来源: 题型:解答题
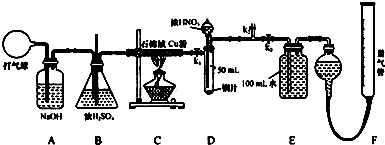
查看答案和解析>>
科目: 来源: 题型:解答题

 .
.查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com