
科目: 来源: 题型:选择题
| A. | 1.6g | B. | (a-1.6)g | C. | (a-3.2)g | D. | 无法计算 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol甲烷的质量与甲烷的摩尔质量相等 | |
| B. | 28 g氮气与40 g氩气所含的原子数目相等,都是NA个 | |
| C. | 2.3 g钠和过量氧气反应,失去的电子数为0.1NA | |
| D. | 18 g重水(D2O)所含的电子数为10NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1molHgO与0.3molHg | B. | 0.2molHgO与0.2mol Hg | ||
| C. | 0.4molHgO与0.2mol O2 | D. | 0.4molHgO |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 物质的量的单位是mol | |
| B. | 物质的量和时间一样,也是一种物理量 | |
| C. | 通过物质的量建立起宏观数量和微观粒子数量的联系 | |
| D. | 物质的量大的物质所占体积一定就大于物质的量小的物质 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2(s)+2Fe3+(aq)═2Fe(OH)3(s)+3Mg2+(aq) | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| C. | 已知:酸的强弱H2CO3>HClO>HCO3-,则:2ClO-+CO2(少量)+H2O═CO32-+2HClO | |
| D. | 将足量的NaHCO3溶液加入少量澄清石灰水中:Ca2++OH-+HCO3-═CaCO3↓+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 | |
| B. | 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 | |
| C. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
查看答案和解析>>
科目: 来源: 题型:解答题
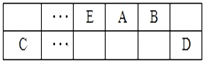
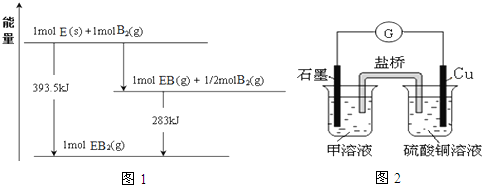
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过氧化钠的电子式:Na${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$Na | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: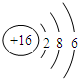 | |
| D. | 间二甲苯的结构简式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com