
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
 向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )
向体积为0.5L的AlCl3溶液中逐渐加入某浓度的NaOH溶液,得到的沉淀随NaOH溶液体积的变化如图所示.下列结果不正确的是( )| A. | 反应过程中,沉淀最多时的质量为78g | |
| B. | 反应过程中,Al3+离子有$\frac{1}{3}$转化为Al(OH)3沉淀,则加入的NaOH溶液的体积可能为3.5L | |
| C. | AlCl3溶液的浓度为2.0 mol/L | |
| D. | 当V(NaOH)=4.0 L时,得到的溶液中Na+、Cl-浓度一定不相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | 杂质 | 除杂质的方法 | |
| A | SiO2 | CaCO3 | 过量稀硫酸、过滤 |
| B | 铜粉 | 铝粉 | 过量CuCl2溶液、过滤 |
| C | FeCl3溶液 | FeCl2 | 通入适量氯气 |
| D | SO2 | HC1 | 通过NaHSO3溶液的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 能使品红褪色 | |
| B. | 能使湿润的蓝色石蕊试纸变红 | |
| C. | 通入足量的NaOH溶液中,再滴入BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸 | |
| D. | 通入稀溴水中能使溴水褪色,得澄清溶液,再滴加Ba(NO3)2溶液有白色沉淀,该沉淀不溶于硝酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
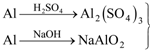 →Al(OH)3.
→Al(OH)3.| A. | 甲、乙消耗的原料同样多 | B. | 乙消耗的原料最少 | ||
| C. | 丙消耗的原料最少 | D. | 三者消耗的原料同样多 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③⑤⑥ | C. | ①③④⑤⑥ | D. | .全部 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③ | B. | ③② | C. | ③① | D. | ①②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 只有① | B. | 只有①②③ | C. | 只有②③ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com