
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4 NH3•H2O═AlO2-+4NH4+ | |
| D. | 向CuSO4溶液中加入Na:2 Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由于明矾可提高米线的“劲道”,所以在制作米线时可大量使用 | |
| B. | 一些火锅店、煲汤店食用“一滴香”,由“一滴香”制成的汤对人体无害 | |
| C. | 过氧化钙具有强氧化性,对面粉有漂白、防霉作用,可在面粉中放心使用 | |
| D. | “地沟油”严重危害人体健康,应从源头把关,禁止其流入市场 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | pH | … |
| 1 | 250 | m | T1 | X | … |
| 2 | 250 | m | T2 | Y | … |

查看答案和解析>>
科目: 来源: 题型:解答题

 ;
; ;
; CH2CH2OOCH、
CH2CH2OOCH、 COOCH2CH3、
COOCH2CH3、 CH2COOCH3、
CH2COOCH3、 00CCH2CH3.
00CCH2CH3. CH(CH3)OOCH.
CH(CH3)OOCH.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
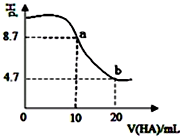 室温下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | HA为强酸 | |
| B. | a、b两点所示溶液中水的电离程度相同 | |
| C. | b点所示溶液中c(A-)>c(HA) | |
| D. | pH=7时,c(Na+)=c(A-)+c(HA) |
查看答案和解析>>
科目: 来源: 题型:选择题
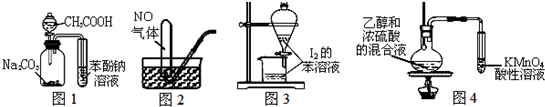
| A. | 图1证明酸性:CH3COOH>H2CO3>苯酚 | |
| B. | 图2用排水法收集NO | |
| C. | 图3萃取碘水中I2,分出水层后的操作 | |
| D. | 图4验证乙烯的生成 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A. | 向AgCl悬浊液中加入稀的NaI溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B. | 在某溶液中加KSCN | 溶液显红色 | 该溶液中有Fe3+,无Fe2+ |
| C. | 在酒精灯上加热铝箔 | 铝箔熔化滴落下来 | 金属铝的熔点较低 |
| D. | 将气体通入澄清石灰水 | 溶液变浑浊 | 该气体一定是CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com