
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
 氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)(△H<0)
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g)?Si3N4(s)+6CO(g)(△H<0)查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl,④NH3•H2O,c(NH4+)由大到小的顺序是:①>③>②>④ | |
| B. | 常温时,将等体积的盐酸和氨水混合后pH=7,则c (NH4+)>c (Cl-) | |
| C. | 0.2 mol•L-1Na2CO3溶液中:c (CO32-)+c (HCO3-)+c (H2CO3)=0.2 mol•L-1 | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到酸性溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 向氯水中加CaCO3后,溶液漂白性增强 | |
| C. | 将氯化铁溶液加热蒸干最终得不到氯化铁固体 | |
| D. | 增大压强,有利于SO2和O2反应生成SO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 无色溶液:Cu2+、H+、Cl-、HSO${\;}_{3}^{-}$ | |
| B. | 滴加石蕊试液显红色的溶液:Na+、NH${\;}_{4}^{+}$、Fe2+、NO${\;}_{3}^{-}$ | |
| C. | Na2CO3溶液:K+、Fe3+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | |
| D. | pH=12的溶液:Na+、K+、SiO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向AgCl沉淀中滴入稀KI溶液白色沉淀变黄,说明Ksp(AgCl)大于Ksp(AgI) | |
| B. | 盐溶液中加入NaOH微热,产生使湿润的红色石蕊试纸变蓝的气体,则一定是铵盐 | |
| C. | 向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,则可用CCl4从碘水中萃取碘单质 | |
| D. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳酸的电离方程式:H2CO3?2H++CO32- | |
| B. | 硫化钠水解:S2-+2H2O?H2S+2OH- | |
| C. | 往AgI悬浊液中滴加Na2S饱和溶液:2Ag+ (aq)+S2-(aq)=Ag2S(s) | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
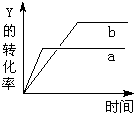 反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )
反应 X(气)+Y(气)?2Z(气)△H<0,在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是( )| A. | 加入催化剂 | B. | 增大压强 | C. | 降低温度 | D. | 增大Y的浓度 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升高温度能使FeCl3溶液中的H+浓度增大 | |
| B. | 在室温下能自发进行的反应,其△H一定小于0 | |
| C. | 溶液呈中性的盐不一定是强酸和强碱生成的盐 | |
| D. | 常温下,0.005mol•L-1Ba(OH)2溶液pH为12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com