
科目: 来源: 题型:选择题
| A. | 干冰升华和液氯气化时要破坏不同的微粒间作用力 | |
| B. | CO2和SiO2具有相同的化学键类型和晶体类型 | |
| C. | 水结成冰体积膨胀、密度变小,这一事实与水分子间存在氢键有关 | |
| D. | 盐酸能电离出氢离子和氯离子,所以HCl中存在离子键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Mg 2+的结构示意图: | B. | NH3分子的电子式: | ||
| C. | H2S的结构式:H-S-H | D. | CH4分子的比例模型: |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 12C和14C | B. | 金刚石与石墨 | ||
| C. | CH3CHO与 | D. | CH3CHCH2CH3与CH3CH2CH2CHCH3 |
查看答案和解析>>
科目: 来源: 题型:解答题
 化学电池在通讯、交通及日常生活中有着广泛的应用.
化学电池在通讯、交通及日常生活中有着广泛的应用.查看答案和解析>>
科目: 来源: 题型:解答题
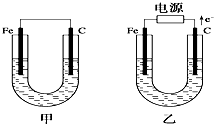 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电解饱和食盐水时,一般用铁作阳极,碳作阴极 | |
| B. | 电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 | |
| C. | 对于冶炼像钠、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 | |
| D. | 电解精炼铜时,用纯铜板作阴极,粗铜板作阳极 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学反应过程中,分子的种类和数目一定发生改变 | |
| B. | 对一可逆反应,其他条件不变时,升高温度,平衡常数K一定增大 | |
| C. | 化学反应过程中,一定有化学键的断裂和形成 | |
| D. | 放热反应的反应速率,一定比吸热反应的反应速率大 |
查看答案和解析>>
科目: 来源: 题型:解答题
 某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、SO42-,现每次取该溶液100.00ml溶液进行以下实验:
某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、SO42-,现每次取该溶液100.00ml溶液进行以下实验:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25mL 0.1mol•L-1的BaCl2溶液 | B. | 50mL 0.3mol•L-1的NaCl溶液 | ||
| C. | 50 mL0.3mol•L-1的FeCl3溶液 | D. | 75 mL 0.1mol•L-1的KCl溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com