
科目: 来源: 题型:选择题
| A. | 红棕色的NO2加压后颜色先变深再变浅 | |
| B. | H2、I2、HI混合气体加压后颜色变深 | |
| C. | 合成氨时高温、高压对合成氨有利 | |
| D. | 醋酸溶液稀释时,溶液pH增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烯和聚乙烯都能使酸性KMnO4溶液褪色 | |
| B. | 等质量的乙烯与聚乙烯完全燃烧,产生的CO2质量相等 | |
| C. | 乙醇和乙醚(CH3CH2OCH2CH3)互为同分异构体 | |
| D. | 乙炔与苯互为同系物 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
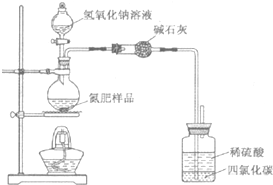 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:| 氢氧化钠溶液/mL | 40.00 | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2、64、24 | B. | 16、50、24 | C. | 32、50、12 | D. | 64、2、24 |
查看答案和解析>>
科目: 来源: 题型:解答题

 (R1~R4表示氢或烃基)
(R1~R4表示氢或烃基) .
. .
. (其中任一种).
(其中任一种).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用氨水鉴别Al3+、Mg2+和Ag+ | |
| B. | 用Ba( NO3)2溶液鉴别Cl-、$SO_4^{2-}$和$CO_3^{2-}$ | |
| C. | 用核磁共振氢谱鉴别l-溴丙烷和2-溴丙烷 | |
| D. | 用KMnO4酸性溶液鉴别CH3CH═CHCH2OH和CH3CH2CH2CHO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 少量白磷贮存于水中,切割时要在水下进行 | |
| B. | 液溴直接保存于磨口玻璃塞的细口棕色瓶中 | |
| C. | KOH溶液存放在磨口玻璃塞的广口瓶中 | |
| D. | 少量金属钠存放在无水乙醇中 |
查看答案和解析>>
科目: 来源: 题型:解答题
 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.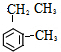 .
. (假设按1:1:1的单体比例合成).
(假设按1:1:1的单体比例合成). ,制取写出相关的化学方程式:
,制取写出相关的化学方程式: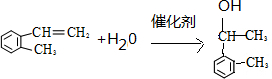 、
、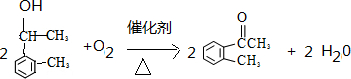 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com