
科目: 来源: 题型:解答题
 《Nature》报道了我国科学家通过测量化石中26AI和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”.回答下列问题:
《Nature》报道了我国科学家通过测量化石中26AI和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”.回答下列问题:| 仪器代号 | 所装试剂 | 装置作用 |
| A | 石灰石和1mol/L硝酸. | 制取CO2证明硝酸比碳酸强 |
| C | 饱和碳酸氢钠溶液 | 除去CO2中的硝酸蒸气 |
| C | 硅酸钠溶液 | 证明碳酸强于硅酸 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
 科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )
科学家根据自然界存在的N2制取出N3,又陆续制取出N5+、N4H44+等离子.已知N4H44+的空间构型如图,下列说法正确的是( )| A. | N3和N2互为同位素 | |
| B. | 7.0gN5+离子含有34×6.02×1022个电子 | |
| C. | N5+中氮、氮原子间形成离子键 | |
| D. | N4H44+的4个H共平面 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)→C(石墨);△H=-1.9KJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=+285.8KJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l);△H=-53.7KJ/mol,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于53.7KJ/mol |
查看答案和解析>>
科目: 来源: 题型:填空题
 .
. .
. ,乙烷的结构简式CH3-CH3.
,乙烷的结构简式CH3-CH3. .
.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在元素周期表中,s区、d区和ds区的元素都是金属 | |
| B. | 可能存在核外电子排布为1s22s22p63s23p64s24p1的原子 | |
| C. | 能层序数越大,s原子轨道的半径越大 | |
| D. | 在同一能级上运动的电子,其运动状态一定相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | N2的结构式: | |
| B. | 次氯酸的结构式为:H-Cl-O | |
| C. | 硫离子的核外电子排布式:1s22s22p63s23p6 | |
| D. | NH3的电子式: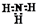 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com