
科目: 来源: 题型:解答题
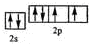 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2O+H2O?H3O++OH- | B. | Cu(NO3)2═Cu2++NO3- | ||
| C. | H2CO3?2H++CO32- | D. | NaOH?Na++OH- |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 检验Cl-离子的试剂是硝酸银和硝酸 | |
| B. | 检验SO42-离子的试剂是氯化钡和盐酸 | |
| C. | 检验CO32-离子的试剂是盐酸和澄清石灰水 | |
| D. | 向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO42- |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
 实验室利用饱和NaNO2溶液(12mol/L)和NH4Cl溶液加热制备N2.
实验室利用饱和NaNO2溶液(12mol/L)和NH4Cl溶液加热制备N2.
查看答案和解析>>
科目: 来源: 题型:解答题




 ;W2Z
;W2Z .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 的流程(无机试剂任用).有机合成流程示例如下:
的流程(无机试剂任用).有机合成流程示例如下:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com